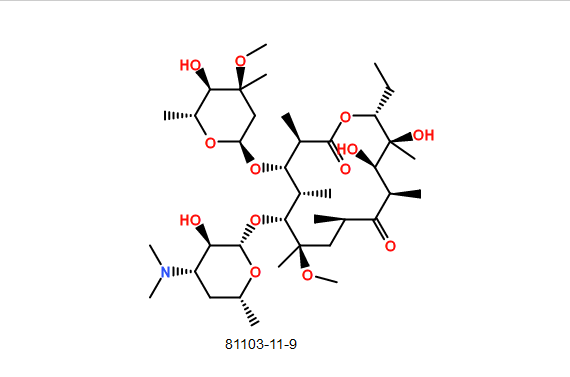
克拉霉素是红霉素的衍生物,20世纪90年代初由日本大正公司开发成功,并以商品名Clarith注册。尔后,大正公司首先将其技术转让给美国雅培公司生产。1990年在爱尔兰、义大利上市,1991年10月获FDA批准定为IB类新药上市,商品名Biaxin,1993年以Klacid在中国香港上市,在欧洲和亚洲的商品名为克拉仙,已在全球50多个国家上市,市场用量稳步增长,并在临床中发挥了重要作用。克拉霉素及其片剂、目前生产的剂型还有颗粒剂、分散片、缓释片、注射剂和乾混悬剂。
基本介绍
- 药品名称:克拉霉素
- 别名:克拉仙; 克拉红霉素;6-0-甲基红霉素A;6氧甲基红霉素;甲红霉素;甲氧基红霉素;克红霉素;
- 外文名称:6-0-MethylerythromycinA、Claricid、Klaricid、6-0-MethylerythromycinA、Claricid、Klaricid
- 药品类型:西医药物
- 发明国家:日本
- 商品名:Clarith
- 简写:CLARY
化合物简介
基本信息
中文名称:克拉霉素
中文别名:克拉仙; 克拉红霉素;6-0-甲基红霉素A;6氧甲基红霉素;甲红霉素;甲氧基红霉素;克红霉素;沃克;甲力;卡碧士;卡斯迈欣;莱欣;利迈先
英文名称:clarithromycin
英文别名:BIAXIN;Claris; te-03; Clarithromycin;6-0-MethylerythromycinA;Claricid;6-0-MethylerythromycinA;Claricid;Klaricid
CAS号:81103-11-9
分子式:C38H69NO13
分子量:747.95300
精确质量:747.47700
PSA:182.91000
LogP:2.43970
物化性质
外观与性状:本品为白色或类白色结晶性粉末;无臭,味苦。本品在三氯甲烷中易溶,在丙酮或乙酸乙酯中溶解,在甲醇或乙醇中微溶,在水中不溶。
密度:1.18 g/cm3
熔点:217-220ºC
沸点:805.5ºC at 760 mmHg
闪点:440.9ºC
稳定性:冷藏
储存条件:密封保存在原始容器里
安全信息
海关编码:29419000
危险类别码:R22
安全说明:S26; S36
RTECS号:KF4997000
危险品标誌:Xi; Xn
生产方法
1.以红霉素为原料,水解脱去氨基上的一个甲基,再和氯甲酸苄酯反应,对5位侧链四氢吡喃环上的羟基和氨基进行保护,然后在二甲亚碸和四氢呋喃中和碘甲烷反应,对6位上的羟基进行甲基化,再催化氢解脱去保护基,和甲醛反应对氨基进行羟甲基化,最后还原为甲基,即为克拉霉素。
2.(1)红霉素A肟(019-2)的製备在反应瓶中加入无水乙醇50ml和红霉素(019-1)10.0g(13.6mmol),搅拌下滴加冰醋酸,溶液呈透明后,加入盐酸羟胺7.0g(100.0mmol),在适当的酸硷缓冲体系下,升温至50~60 oC ,搅拌反应8~24h. TLC跟蹤确认反应达终点后,终止反应.冷至室温,过滤除去无机盐,滤液减压蒸发至乾,得白色固体.将该固体溶于20ml乙酸乙酯中,搅拌下加入4mol/L NaOH溶液,调至pH>=12.静置分层,有机层用适量水洗涤2~3次后,真空浓缩至乾,得白色固体,乾燥至恆重,得019-2 9.98g,收率99.9%.含019-2 93.5%,其中E-肟 82.9%,Z-肟10.6%,红霉素降解产物红霉素A 8,9-脱水-6,9-半缩酮<=2%(HPLC法).将019-2重结晶得019-2.纯品,收率95.6%。
(2)2’,4”-O-双(三甲基硅)红霉素A 9-O-(1-乙氧基环己基)肟[2’,4’’-Obis(trimethylsilyl)-eryth-romycin A 9-O91-ethoxycyclohexyl]oxime](019-4)的製备在反应瓶中加入乙腈500ml、019-2 50.0g(67mmol)和盐酸吡啶15.0g(134mmol),搅拌下加入1-乙氧基环己烯(EOCHE)30.0ml(223mmol),在室温(28 oC)下搅拌反应,反应液逐渐变清无色,3h后全部转化为红霉素A9-O-(1-乙氧基环己基)肟(019-3),再加入1,1,1,3,3,3-六甲基二硅氨烷(HMDS)50.0ml (240mmol),反应液立即呈白色浊态.搅拌反应2h后,加入4mol/L NaOH溶液调至PH>=10,用乙酸乙酯(200ml*2)提取,有机相用水洗,饱和食盐水洗,无水MgSO4乾燥过夜.过滤,滤液减压蒸除溶剂得019-4,mp108~110 oC.
(3)2’,4’’-O-双(三甲基硅)6-O-甲基红霉素A 9-O-(1-乙氧基环己基)肟[2’,4’’-Obis(trimethylsilyl)-6-O-methylerythromycin A 9-O-(1-ethoxycyclohexyl)oxime](019-5)的製备。在反应瓶中加入DMSO/THF(体积比1:1)400ml和019-4(上步一批量),搅拌溶解,再加入碘甲6.0ml(96mmol)和82%的KOH粉末6.0g(88mmol),于0 oC 搅拌反应1h.加水200ml,用乙酸乙酯提取(200ml*2),无水MgSO4乾燥有机相,过滤,滤液蒸除溶剂得019-5,mp127~129 oC 。直接用于下步反应。
(4)克拉霉素(019)的合成在反应瓶中加入250ml乙醇和水,再加入019-5(上步一批得量),搅拌溶解,搅拌下加入甲酸5.0ml(132mmol),反应数小时后,TLC跟蹤显示得6-O-甲基红霉素A 9-O-(1-乙氧基环己基)肟和6-O-甲基红霉素 A-9-肟,再补加NaHSO3 50.0g(480mmol),搅拌加热至回流,反应2h.用4mol/L的NaOH溶液调至PH>=10,析出白色固体019,用乙醇重结晶得精品019 24.7g,以红霉素A计总收率达49.5%,mp222~225 oC .
2.(1)红霉素A肟(019-2)的製备在反应瓶中加入无水乙醇50ml和红霉素(019-1)10.0g(13.6mmol),搅拌下滴加冰醋酸,溶液呈透明后,加入盐酸羟胺7.0g(100.0mmol),在适当的酸硷缓冲体系下,升温至50~60 oC ,搅拌反应8~24h. TLC跟蹤确认反应达终点后,终止反应.冷至室温,过滤除去无机盐,滤液减压蒸发至乾,得白色固体.将该固体溶于20ml乙酸乙酯中,搅拌下加入4mol/L NaOH溶液,调至pH>=12.静置分层,有机层用适量水洗涤2~3次后,真空浓缩至乾,得白色固体,乾燥至恆重,得019-2 9.98g,收率99.9%.含019-2 93.5%,其中E-肟 82.9%,Z-肟10.6%,红霉素降解产物红霉素A 8,9-脱水-6,9-半缩酮<=2%(HPLC法).将019-2重结晶得019-2.纯品,收率95.6%。
(2)2’,4”-O-双(三甲基硅)红霉素A 9-O-(1-乙氧基环己基)肟[2’,4’’-Obis(trimethylsilyl)-eryth-romycin A 9-O91-ethoxycyclohexyl]oxime](019-4)的製备在反应瓶中加入乙腈500ml、019-2 50.0g(67mmol)和盐酸吡啶15.0g(134mmol),搅拌下加入1-乙氧基环己烯(EOCHE)30.0ml(223mmol),在室温(28 oC)下搅拌反应,反应液逐渐变清无色,3h后全部转化为红霉素A9-O-(1-乙氧基环己基)肟(019-3),再加入1,1,1,3,3,3-六甲基二硅氨烷(HMDS)50.0ml (240mmol),反应液立即呈白色浊态.搅拌反应2h后,加入4mol/L NaOH溶液调至PH>=10,用乙酸乙酯(200ml*2)提取,有机相用水洗,饱和食盐水洗,无水MgSO4乾燥过夜.过滤,滤液减压蒸除溶剂得019-4,mp108~110 oC.
(3)2’,4’’-O-双(三甲基硅)6-O-甲基红霉素A 9-O-(1-乙氧基环己基)肟[2’,4’’-Obis(trimethylsilyl)-6-O-methylerythromycin A 9-O-(1-ethoxycyclohexyl)oxime](019-5)的製备。在反应瓶中加入DMSO/THF(体积比1:1)400ml和019-4(上步一批量),搅拌溶解,再加入碘甲6.0ml(96mmol)和82%的KOH粉末6.0g(88mmol),于0 oC 搅拌反应1h.加水200ml,用乙酸乙酯提取(200ml*2),无水MgSO4乾燥有机相,过滤,滤液蒸除溶剂得019-5,mp127~129 oC 。直接用于下步反应。
(4)克拉霉素(019)的合成在反应瓶中加入250ml乙醇和水,再加入019-5(上步一批得量),搅拌溶解,搅拌下加入甲酸5.0ml(132mmol),反应数小时后,TLC跟蹤显示得6-O-甲基红霉素A 9-O-(1-乙氧基环己基)肟和6-O-甲基红霉素 A-9-肟,再补加NaHSO3 50.0g(480mmol),搅拌加热至回流,反应2h.用4mol/L的NaOH溶液调至PH>=10,析出白色固体019,用乙醇重结晶得精品019 24.7g,以红霉素A计总收率达49.5%,mp222~225 oC .
用途
属大环内酯类抗生素,用于治疗上、下呼吸道感染,皮下软组织感染等。
药典标準
鉴别
(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱应与对照的图谱(《药品红外光谱集》756图)一致,必要时取供试品与对照品适量,溶于三氯甲烷,于室温挥发至乾,经真空乾燥后取残渣测定,应与对照品的图谱一致。
检查
1硷度
取本品,用水-甲醇(19:1)混合溶液製成每1ml中含2mg的混悬液,依法测定(2010年版药典二部附录Ⅵ H),pH值应为7.5~10.0。
2结晶性
取本品,依法检查(2010年版药典二部附录ⅨD),应符合规定。
3有关物质
取本品适量,加流动相溶解并稀释製成每1ml中含1.0mg的溶液,作为供试品溶液;精密量取5ml,置100ml量瓶中,用流动相稀释至刻度,摇匀,作为对照溶液。照含量测定项下的色谱条件,取对照溶液20μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的50%。精密量取供试品溶液与对照溶液各20μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.5倍(2.5%);各杂质峰面积的和不得大于对照溶液主峰面积的1.2倍(6.0%)。
4水分
取本品,加10%咪唑无水甲醇溶液溶解,照水分测定法(2010年版药典二部附录ⅧM第一法 A)测定,含水分不得过2.0%。
5炽灼残渣
取本品1.0g,依法检查(2010年版药典二部附录Ⅷ N),遗留残渣不得过0.3%。
6重金属
取炽灼残渣项下遗留的残渣,依法检查(2010年版药典二部附录Ⅷ H第二法),含重金属不得过百万分之二十。
含量测定
照高效液相色谱法(2010年版药典二部附录ⅤD)测定。
1色谱条件与系统适用性试验
用十八烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(取磷酸二氢钾9.11g,加水溶解并稀释至1000ml,加三乙胺2ml,用磷酸调节pH值至5.5)-乙腈(600:400)为流动相;检测波长为210nm;柱温45℃。理论板数按克拉霉素峰计算不低于3000;拖尾因子不得过2.0;克拉霉素峰与相邻杂质峰的分离度应符合要求。
2测定法
取本品适量,精密称定,加流动相溶解并定量稀释製成每1ml中约含0.35mg的溶液,精密量取20μl注入液相色谱仪,记录色谱图;另取克拉霉素对照品适量,同法测定。按外标法以峰面积计算,即得。
类别
大环内酯类抗生素。
贮藏
遮光,密封保存。
製剂
(1)克拉霉素片 (2)克拉霉素胶囊 (3)克拉霉素颗粒
药物说明
药理作用
该品属14元环大环内酯类抗生素。抗菌谱与红霉素、罗红霉素等相同,但对革兰阳性菌如链球菌属、肺炎球菌、葡萄球菌的抗菌作用略优,且对诱导产生的红霉素耐药菌株亦具一定抗菌活性。克拉霉素及其在体内的代谢产物对流感桿菌的抗菌作用增强。该品对淋球菌、李斯忒菌、空肠弯曲菌也有一定作用,而对嗜肺军团菌、肺炎支原体、沙眼衣原体、溶脲脲原体等的作用比红霉素为强,在近年开发的新品种中作用较突出,MIC90约0.008~0.12mg/L。此外,对包柔螺旋体、鸟分枝桿菌、鼠弓形体等均具一定活性,且大多优于其他品种。除对厌氧球菌具较强抗菌作用外,对脆弱类桿菌的作用优于红霉素等该品对金葡菌、化脓性链球菌、流感桿菌等的抗生素后效作用明显强于红霉素。本药属大环内酯类抗生素,其机制是通过阻碍细胞核蛋白50S亚基的联结,抑制蛋白质的合成而产生抑菌作用。本药对革兰氏阳性菌如金黄色葡萄球菌、链球菌、肺炎球菌等有抑制作用,对部分革兰氏阴性菌如流感嗜血桿菌、百日咳桿菌、淋病双球菌、嗜肺军团菌和部分厌氧菌如脆弱拟桿菌、消化链球菌、痤疮丙酸桿菌等也有抑制作用。此外对支原体也有抑制作用。本药特点为在体外抗菌活性与红霉素相似,但在体内对部分细菌如金黄色葡萄球菌、链球菌、流感嗜血桿菌等抗菌活性比红霉素强。与红霉素之间有交叉耐药性。
药代动力学
该品对胃酸稳定,口服吸收好。单剂顿服100mg后2h达峰浓度,为0.35μg/ml;而顿服1200mg后的峰浓度可达3.97μg/ml。该品能迅速分布至各种组织中,肺组织中的药物浓度达17.5μg/g;在扁桃体、鼻黏膜、皮肤中的浓度约为同期血药浓度的2~6倍。药物在细胞内与细胞外的浓度之比为16:4。蛋白结合率为42%~70%。主要经粪及尿排泄。消除半减期为2.6~4.4h。轻度肾功能不全者、或老年人、或轻度至中度肝功能不全者无需调整用药剂量。 克拉霉素
克拉霉素
 克拉霉素
克拉霉素适应症
主要用于敏感细菌所致的上、下呼吸道,包括扁桃体炎、咽喉炎、鼻窦炎、支气管炎、肺炎等、皮肤、软组织感染、脓疖、丹毒、毛囊炎、伤口感染等,疗效与其他大环内酯类相仿。该品也可用于沙眼衣原体或溶脲脲原体所致生殖泌尿系感染、爱滋病患者的非典型分支桿菌感染等。 克拉霉素
克拉霉素
 克拉霉素
克拉霉素用法用量
成人每12h服250mg,严重患者剂量可增至每12h500mg;疗程据感染程度而定,一般为7~14日。肌酐清除率低于0.501ml/1.73平方米·秒者剂量减半。儿童剂量:每次7.5mg/kg,每日2次,最高剂量不超过每日500mg。轻症:每次250mg,重症每次500mg,均为12小时1次,疗程7—14日。12岁以上儿童按成人量。12岁以下儿童不套用此药。 荨麻疹
荨麻疹
 荨麻疹
荨麻疹不良反应
1、可见噁心,胃灼热,腹痛腹泻,头痛。暂时性转氨酶升高,停药后可恢复。有胆汁性肝炎的个例。可能出现真菌或具抗药性细菌导致的严重感染,这时应停药,并作相应治疗。可发生过敏反应,轻者为药疹,荨麻疹,重者为过敏症。曾有短暂性中枢神经系统副作用的报告,如焦虑,头晕,失眠,幻觉,恶梦及意识模糊。不良反应有腹泻(3%)、噁心(3%)、味觉改变(3%)、消化不良(2%)、腹痛或不适(2%)、头痛(2%),一般程度较轻。 克拉霉素
克拉霉素
 克拉霉素
克拉霉素2、尚可见ALT、AST、LDH、硷性磷酸酶、胆红素升高(均<1%);白细胞减少(<1%)、凝血酶原时间延长(1%)、BUN升高(4%)、血清肌酐值升高(<1%)等。
禁忌症
对大环内酯类药物过敏者,孕妇,哺乳妇女,严重肝肾功能低下者,心律失常,心动过缓,Q-T间期延长,缺铁性心脏病,充血性心力衰竭及水电解质紊乱者禁用或慎用.该品主要在肝内代谢和排泄,因此肝功能不全者、严重肾功能不全者和65岁以上老年人用药时需特别注意不良反应。服药过量时可出现胃肠道功能紊乱和全身症状、可予洗胃及支持疗法。血透和腹膜透析都不能清除该品,故应从速排除尚未吸收的药物(如洗胃),并给予对症治疗。孕妇禁用(该品在动物胚胎中浓度为人血清的2—17倍)。哺乳妇慎用(宜暂停哺乳)。
过量处理
当服用大剂量的克拉霉素时,可能有胃肠不适。因过量引起的症状应迅速洗胃并适当给予支持疗法。至今无报告过用血或腹膜透析来清除克拉霉素。但有必要儘快排除未被吸收的药物,同时採取适当的对症治疗。
药物相互作用
该品可干扰卡马西平代谢,使后者血药浓度明显增高,二者合用时应监测血药浓度,必要时调整用药剂量。与茶硷合用可使茶硷血浓度增高,但一般不必调整茶硷的剂量。该品可使下列联合套用的药物血药浓度发生变化:地高辛(上升)、茶硷(上升)、口服抗凝血药(上升)、麦角胺或二氢麦角硷(上升)、三唑侖(上升)而显示更强的作用。对于卡马西平、环胞霉素、己巴比妥、苯妥英等也可有类似的阻滞代谢而使作用加强。 克拉霉素
克拉霉素
 克拉霉素
克拉霉素製剂/规格
⑴克拉霉素片⑵克拉霉素胶囊
乾混悬剂
英文名ClarithromycinforSuspension,类别西医药物
适应症
适用于克拉霉素敏感菌所引起的下列感染:
1、鼻咽感染:扁桃体炎、咽炎、鼻窦炎。
2、下呼吸道感染:急性支气管炎、慢性支气管炎急性发作和肺炎。
3、皮肤软组织感染:脓疱病、丹毒、毛囊炎、疖和伤口感染。
4、急性中耳炎、肺炎支原体肺炎、沙眼衣原体引起的尿道炎及宫颈炎等。
5、也用于军团菌感染,或与其他药物联合用于鸟分枝桿菌感染、幽门螺桿菌感染的治疗。
用法用量
成人口服,常用量一次250mg,每12小时1次;重症感染者一次500mg,每12小时1次。根据感染的严重程度应连续服用6~14日。儿童口服,6个月以上的儿童,按体重一次7.5mg/kg,每12小时1次。或按以下方法给药:体重8~11kg,一次62.5mg,每12小时1次;体重12~19kg,一次125mg,每12小时1次;体重20~29kg,一次187.5mg,每12小时1次;体重30~40kg,一次250mg,每12小时1次;根据感染的严重程度应连续服用5~10日。
不良反应
1、主要有口腔异味(3%),腹痛、腹泻、噁心、呕吐等胃肠道反应(2%~3%),头痛(2%),血清氨基转移酶短暂升高。
2、可能发生过敏反应,轻者为药疹、荨麻疹,重者为过敏及Stevens—Johnson症。
3、偶见肝毒性、艰难梭菌引起的假膜性肠炎。
4、曾有发生短暂性中枢神经系统副作用的报告,包括焦虑、头昏、失眠、幻觉、恶梦或意识模糊,然而其原因和药物的关係仍不清楚。
禁忌
1、对该品或大环内酯类药物过敏者禁用。
2、孕妇、哺乳妇女期禁用。
3、严重肝功能损害者、水电解质紊乱患者、服用特非那丁治疗者禁用。
4、某些心脏病(包括心律失常、心动过缓、Q-T间期延长、缺血性心脏病、充血性心力衰竭等)患者禁用。
注意事项
1、该品可空腹口服,也可与食物或牛奶同服,与食物同服不影响其吸收。6.血液或腹膜透析不能降低该品的血药浓度。
2、6个月以下儿童的疗效和安全性尚未确定。动物实验中该品对胚胎及胎儿有毒性作用,同时该品及其代谢产物可进入母乳中,故孕妇及哺乳期妇女禁用。老年人的耐受性与年轻人相仿。 蛋白质
蛋白质
 蛋白质
蛋白质3、该品与红霉素及其他大环内酯类药物之间有交叉过敏和交叉耐药性。
4、与别的抗生素一样,可能会出现真菌或耐药细菌导致的严重感染,此时需要中止使用该品,同时採用适当的治疗。
5、肝功能损害、中度至严重肾功能损害者慎用。
6、肾功能严重损害(肌酐清除率小于30ml/分钟)者,须作剂量调整。常用量为一次250mg,一日1次;重症感染者首剂500mg,以后一次250mg,一日2次。
过量处理
当服用大剂量的克拉霉素时,可能有胃肠不适。因过量引起症状时应迅速洗胃并适当给予支持疗法。
相互作用
1、大环内酯类抗生素能改变特非那丁的代谢而升高其血浓度,导致心律失常如室性心动过速、室颤和充血性心力衰竭。2.该品对氨茶硷、茶硷的体内代谢略有影响,一般不需要调整后者的剂量,但氨茶硷、茶硷套用剂量偏大时需监测血浓度。
3、与氟康唑合用会增加该品血浓度。
4、该品与HMG—CoA还原酶抑制药(如洛伐他丁和辛伐他丁)合用,极少有横纹肌溶解的报导。
5、该品与西沙必利、匹莫齐特合用会升高后者血浓度,导致Q—T间期延长,心率失常如室性心动过速、室颤和充血性心力衰竭。与阿司咪唑合用会导致Q—T间期延长,但无任何临床症状。
6、该品可轻度升高卡马西平的血药浓度,两者合用时需对后者作血药浓度监测。
7、该品与地高辛合用会引起地高辛血浓度升高,应进行血药浓度监测。
8、HⅣ感染的成年人同时口服该品和齐多夫定时,该品会干扰后者的吸收使其稳态血浓度下降,应错开服用时间。
9、与利托那韦合用该品代谢会明显被抑制,故该品每天剂量大于1g时,不应与利托那韦合用。
10、与其他大环内酯类抗生素相似,该品会升高需要经过细胞色素P450系统代谢的药物的血清浓度(如阿司咪唑、华法林、麦角生物硷、三唑侖、咪达唑侖、环胞素、奥美拉唑、雷尼替丁、苯妥因、溴隐亭、阿芬他尼、海索比妥、丙吡胺、洛伐他丁、他克莫司等)。
製剂
⑴1g:0.125g⑵2g:0.125g⑶2g:0.25g
颗粒製剂
适应症
适用于克拉霉素敏感菌所引起的下列感染:1.鼻咽感染:扁桃体炎、咽炎、鼻窦炎。2.下呼吸道感染:急性支气管炎、慢性支气管炎急性发作和肺炎。3.皮肤软组织感染:脓疱病、丹毒、毛囊炎、疖和伤口感染。4.急性中耳炎、肺炎支原体肺炎、沙眼衣原体引起的尿道炎及宫颈炎等。5.也用于军团菌感染,或与其他药物联合用于鸟分枝桿菌感染、幽门螺桿菌感染的治疗。
不良反应
1.曾有发生短暂性中枢神经系统副作用的报告,包括焦虑、头昏、失眠、幻觉、恶梦或意识模糊,然而其原因和药物的关係仍不清楚。
2.可能发生过敏反应,轻者为药疹、荨麻疹,重者为过敏及Stevens—Johnson症。
3.偶见肝毒性、艰难梭菌引起的假膜性肠炎。
4.主要有口腔异味(3%),腹痛、腹泻、噁心、呕吐等胃肠道反应(2%~3%),头痛(2%),血清氨基转移酶短暂升高。
禁忌
1.对该品或大环内酯类药物过敏者禁用。
2.孕妇、哺乳妇女期禁用。
3.严重肝功能损害者、水电解质紊乱患者、服用特非那丁治疗者禁用。
4.某些心脏病(包括心律失常、心动过缓、Q-T间期延长、缺血性心脏病、充血性心力衰竭等)患者禁用。
注意事项
⒈肝功能损害、中度至严重肾功能损害者慎用。
⒉肾功能严重损害(肌酐清除率小于30ml/分钟)者,须作剂量调整。常用量为一次250mg,一日1次;重症感染者首剂500mg,以后一次250mg,一日2次。
⒊该品与红霉素及其他大环内酯类药物之间有交叉过敏和交叉耐药性。
⒋与别的抗生素一样,可能会出现真菌或耐药细菌导致的严重感染,此时需要中止使用该品,同时採用适当的治疗。
⒌该品可空腹口服,也可与食物或牛奶同服,与食物同服不影响其吸收。6.血液或腹膜透析不能降低该品的血药浓度。
6个月以下儿童的疗效和安全性尚未确定。动物实验中该品对胚胎及胎儿有毒性作用,同时该品及其代谢产物可进入母乳中,故孕妇及哺乳期妇女禁用。老年人的耐受性与年轻人相仿。
过量处理
当服用大剂量的克拉霉素时,可能有胃肠不适。因过量引起症状时应迅速洗胃并适当给予支持疗法。
治疗病例
非淋菌性尿道炎主要由沙眼衣原体(CT)和解脲支原体(Uu)引起,可单独或混合感染。我们于2000年5月至2002年1月套用克拉霉素治疗201例非淋菌性尿道炎,取得满意疗效,现报告如下。
材料与方法
1病例选择所有患者均为门诊就诊者,无严重的内脏疾病,对大环内酯类药物无过敏史;年龄18~52岁,平均26.0±4.8岁;其中男性102例,女性99例;病程最短6天,最长1年半;发病前有婚外性生活史,或配偶有非淋菌病原体感染史。男性主要表现为尿道不适感,痒、刺痛或烧灼感,尿道口红肿或有分泌物,时轻时重;女性主要表现为外阴瘙痒,白带增多,宫颈充血,水肿或糜烂[1]。淋球菌涂片或培养均阴性。所有患者自发病至检查期间未用过药物治疗。
标本採集
于治疗前及治疗后男性取尿道分泌物,女性取宫颈分泌物。用消毒棉拭子伸入尿道或宫颈内2~3cm,停留10~30秒,缓慢旋转2圈并取出含有柱状上皮细胞的棉拭子。
试剂和方法
做CT的PCR检测和Uu培养,201例中CT阳性59例,Uu阳性142例,CT、Uu双重感染29例。
治疗方法
利迈先250mg,每日2次口服,连续15天,停药后複查。
疗效判定
标準痊癒为症状、体徵完全消失,病原体检测阴性;显效为病原体阴转(合併感染者有1种阴转),但症状体徵仍有一项未恢复正常;有效为病情好转,但病原体仍未阴转者;无效为治疗后病情无改善,病原体检测阴性。
克拉霉素
临床疗效临床治癒120例(59.7%),显效68例(33.8%),有效10例(4.98%),无效3例(1.49%),总有效率(痊癒+显效)188例(93.5%),男女患者的临床疗效比较,两者无显着性意义(χ2=0.211,P>0.05)。
病原体检测阴转情况Uu阳性126例,治疗后阴转117例(92.9%);CT阳性75例,治疗后阴转70例(93.3%);总阴转率93.0%,两种病原体的阴转率差异无显着性意义(χ2=0.412,P>0.05)。
不良反应观察治疗期间有5例(2.49%)出现噁心、呕吐、腹部不适等胃肠道反应,8例(3.98%)出现静脉炎,经过热敷及对症处理,未中继治疗,均在较短时间内恢复正常,副反应发生率为6.47%。
讨论克拉霉素
克拉霉素(利迈先)是新一代半合成的大环内酯类抗生素,与细菌细胞核糖体50s亚基结合,抑制细菌蛋白质的合成而起到广泛的抑菌杀菌作用,对革兰阳性菌、阴性菌及厌氧菌等都具有很强的抗菌作用,对衣原体、支原体感染的抗菌活性是大环内酯类抗生素中最强的。克拉霉素体外抗沙眼衣原体活性是红霉素的7~10倍,为强力霉素的4倍。它在体内代谢而产生的14羟产物,具有生物活性,其抗菌谱与克拉霉素本身相同,而且它们在体内的抗菌活性比体外大为提高。
克拉霉素对酸的稳定性比红霉素高800倍,在胃酸中稳定吸收,迅速分布到身体各组织和体液中,在泌尿生殖系统及皮肤软组织中均有较高的浓度。口服250mg,其生物利用度约达50%,人血浆蛋白结合率可达70%。体内分布广泛,组织浓度高,其主要代谢产物14—OH克拉霉素仍具较强的抗菌活性,在剂量250mg每日2次的情况下,药物的血浆浓度在2~3天内达到稳定的峰值状态,5天内自尿排出,占剂量的36%,大大高出其他大环内酯类药物平均6%的水平。
克拉霉素片250mg每日2次,在稳定浓度下其本身的消除半衰期为3.5小时,其活性代谢物14羟克拉霉素为4.7小时,半衰期长,每12小时服1片,从而提高了病人服用的方便性和依从性。从治疗结果上看,克拉霉素治疗非淋菌性尿道炎疗效肯定,总有效率93.5%,病原体阴转率93.0%。克拉霉素治疗非淋菌性尿道炎具有疗效好,疗程较短,给药次数少等优点,安全性好,副作用于少,可供临床套用。其不良反应在临床使用时应注意观察。