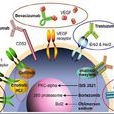
肿瘤分子靶向药物利用肿瘤细胞与正常细胞之间分子生物学上的差异(包括基因、酶、信号转导等不同特性),抑制肿瘤细胞的生长增殖,最后使其死亡。
靶向药物
肿瘤分子靶向药物的作用途径包括调节细胞增殖的信号转导途径、调节血管生成的转导途径、肿瘤抑制基因丢失功能的转导等。
肿瘤分子靶向治疗将比目前的化疗更为有效、副作用更小,是非常有希望的一种肿瘤治疗方法。表皮生长因子受体酪氨酸激酶(EGFR-TK)抑制剂吉非替尼主要治疗肺癌,利妥昔单抗主要用于治疗非霍奇金淋巴瘤,曲妥珠单抗是信号转导抑制剂,用于治疗乳腺癌。治疗慢性粒细胞性白血病和胃肠道基质细胞瘤的是甲磺酸伊马替尼。
靶向机理
目前用于肿瘤靶向治疗研究的常见药物有叶酸、各种抗体以及卟啉等。其中以卟啉最为常见,下面以卟啉为例介绍肿瘤分子靶向机理。
卟啉类化合物对肿瘤组织有特殊的亲和力和较高的选择性,但其分配在肿瘤组织与正常组织中的 数量受多种因素影响,如卟啉的疏水性、配合物的构 型、细胞的选择性结合以及肿瘤组织与正常组织的 渗透性差异。迄今,对于卟啉在肿瘤组织中的聚集 机理还尚无定论,较合理的解释有以下两种
(1)pH值理论
卟啉经被动扩散进入细胞内,其扩散效率随胞外pH值降低而提高。通常,正常组织与肿瘤组织具有不同的pH值(分别为7.0~8.0、5.85~7.68); 且肿瘤组织随代谢加速其胞外pH值降低,大肿瘤细胞的pH值较小,肿瘤细胞低。因此,卟啉可更多地进入肿瘤细胞,完成在肿瘤组织中的优先聚集。
(2)低密度脂蛋白受体理论
单克隆抗体、脂质体、微球体、生长因素、荷尔蒙 及低密度脂蛋白受体,被认为是能提高抗肿瘤药物对肿瘤细胞选择性的抗肿瘤药物运输系统。大量体内、体外实验证明,快速增殖的肿瘤细胞表面含有较多表现出较强活性的低密度脂蛋白受体。许多亲脂性药物分子与低密度脂蛋白受体中心结合,再通过与低密度脂蛋白受体脱辅基蛋白B相互作用的特异性膜受体进入细胞。多数情况下,进入到低密度脂蛋白受体的大脂质囊泡药物能与低密度脂蛋白受体结合,所形成的各种药物一低密度脂蛋白受体複合物能有效地杀伤肿瘤细胞。根据低密度脂蛋白受体理论,肿瘤组织中有较多数量的低密度脂蛋白受体促成卟啉与肿瘤组织更多的结合。以细胞流式方法分析该机理,发现卟啉与低密度脂蛋白受体存在竞争性受体,而这些受体与低密度脂蛋白受 体受体不尽相同,故卟啉与肿瘤细胞的结合受周围 的低密度脂蛋白受体浓度影响较大。寻求控制目标肿瘤细胞低密度脂蛋白受体浓度或者增加低密度 脂蛋白受体数量的有效方法,以提高卟啉与肿瘤细胞的结合,将成为新的癌症治疗策略之一。
药物列表
吉非替尼 | 舒尼替尼 | 尼妥珠单抗 | 贝伐珠单抗 | 曲妥珠单抗 |
克唑替尼 | 埃克替尼 | 阿帕替尼 | 达沙替尼 | 伊马替尼 |
拉帕替尼 | 厄洛替尼 | 依维莫司 | 尼洛替尼 | 索拉非尼 |
利妥昔单抗 | 西妥昔单抗 | |||
Blinatumomab | Daratumumab | Elotuzumab | 阿侖单抗 | 贝利司他 |
Brentuximab vedotin | Dinutuximab | Obinutuzumab | 奥法木单抗 | 伏立诺他 |
罗米地辛 | 帕比司他 | 替伊莫单抗 | 托西莫单抗 | 瑞格非尼 |
Ado-曲妥珠单抗 | 阿雷替尼 | 狄诺塞麦 | 帕博西尼 | 色瑞替尼 |
Cobimetinib | 阿西替尼 | 凡德他尼 | 帕纳替尼 | 索尼吉布 |
Necitumumab | 艾代拉里斯 | 卡博替尼 | 帕尼单抗 | 替西罗莫司 |
Osimertinib | 奥拉帕尼 | 乐伐替尼 | 帕妥珠单抗 | 威罗菲尼 |
阿柏西普 | 博舒替尼 | 雷莫芦单抗 | 帕唑帕尼 | 维莫德吉 |
阿法替尼 | 达拉菲尼 | 尼达尼布 | 曲美替尼 | 依鲁替尼 |
Abemaciclib | BYL719 | Lee011 | Patritumab | 司美替尼 |
Anlotinib | CO-1686 | Lucitanib | Rucaparib | 维利帕尼 |
AZD2014 | EGF816 | MK-1775 | Talazoparib | 多韦替尼 |
AZD4547 | Erismodegib | MK2206 | Tivantinib | 鲁索利替尼 |
AZD5363 | Famitinib | Momelotinib | Neratinib | 安卓建 |
AZD9291 | Fruquintinib | MSC-2363318A | NVP-BGJ398 | 达克替尼 |
Binimetinib | GSK-525762 | Buparlisib | INC280 | |